Ein im Rahmen des Technopolprogramms Niederösterreich gefördertes Forschungsprojekt an der Universität für Weiterbildung Krems entwickelt eine Blutgefäßkammer zur Kultivierung menschlicher Nabelschnurgefäße unter nahezu physiologischen Bedingungen. Ziel ist der Erhalt und die Regeneration der Glykokalyx als Schlüsselstruktur des Endothels. So entsteht ein tierversuchsfreies Testsystem, das neue Einblicke in die Mechanismen von Thrombose und Sepsis ermöglicht und die kardiovaskuläre Forschung entscheidend voranbringt.
Herz-Kreislauf-Erkrankungen zählen weltweit zu den häufigsten Todesursachen und gehen oft mit Veränderungen des Gefäßgewebes einher. Die genauen Mechanismen solcher Erkrankungen, die auf Thrombose oder Sepsis zurückzuführen sind, sind noch weitgehend unerforscht. Wenn diese untersucht werden, dann häufig in Tierversuchen oder In-vitro-Modellen. Letztere können jedoch die In-vivo-Situation nicht abbilden, was zu Tierversuchen führt, die jedoch die physiologischen Bedingungen beim Menschen nicht vollständig wiedergeben können.
Kultivierung menschlicher Nabelschnüre
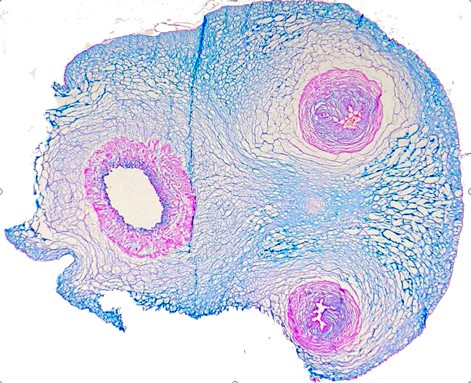
„Das Forschungsprojekt geht von der These aus, dass eine menschliche Nabelschnur, die zwei Arterien und eine Vene hat, in einer selbst entwickelten ‚Blutgefäßkammer‘ kultiviert werden kann. Ziel ist es, die Glykokalyx, eine kohlenhydratreiche Schicht an der Endotheloberfläche, zu erhalten oder zu regenerieren. Damit stünde ein natives menschliches Blutgefäß für Forschungszwecke zur Verfügung“, sagt Christoph Bauer, Projektleiter am Zentrum für Regenerative Medizin der Universität für Weiterbildung Krems. Mit dem Projekt sollen vier Ziele erreicht werden, erstens die Herstellung einer speziellen Kammer für die Kultivierung einer menschlichen Nabelschnur, zweitens die Etablierung von optimalen Kultivierungsbedingungen für eine intakte Glykokalyx und einen aufrechten Zellstoffwechsel, drittens die Weiterentwicklung von Analysemethoden zur Charakterisierung der Glykokalyx und der Endothelzellen und viertens die Etablierung von zwei Modellen zum Ersatz bzw. zur Reduzierung von Tierversuchen in der Thrombose- und Sepsisforschung.
Ein Blick ins „lebende“ Gefäß
Die Blutgefäße der Nabelschnur werden an die Kultivierungskammer angeschlossen und kontinuierlich mit einem endothelialen Nährmedium im Durchfluss inkubiert. Anhand regelmäßig entnommener Gewebeproben werden die intakte Glykokalyx und metabolisch aktive Endothelzellen untersucht. Durchflusszytometrie und Multiplex-Assays überwachen den Einfluss angepasster In-vivo-Kulturbedingungen (z. B. Humanserum, Blutzellen). Sobald die Blutgefäßkammer etabliert ist, wird ein nahezu natives Testsystem für kardiovaskuläre Erkrankungen zur Verfügung stehen, welches mit wie biochemischen (Multiplex-Assay, ELISA), molekularbiologischen (qPCR) und mikroskopischen (SEM, Histologie, konfokale Mikroskopie) Methoden analysiert werden kann. Mit Hilfe der oben genannten Techniken wird ein Glykokalyx-Regenerationsmodell etabliert, welches für die Entwicklung anderer Modelle genutzt werden kann. Dabei soll in einem weiteren Schritt die Sepsis, die häufig durch bakterielle Keime ausgelöst wird, in einem Modell durch Zugabe von Lipopolysaccharid induziert werden. Dies führt zu einem Abbau der Glykokalyx durch entzündliche Mechanismen. Der Abbau kann durch Proteine (z. B. Syndecan-1) oder Enzyme (Metalloproteinasen, Heparinasen) im Überstand nachgewiesen und mittels Elektronenmikroskopie (REM) sichtbar gemacht werden.
Tierversuchsfreie Erforschung von Blutgefäßerkrankungen
Die neu entwickelte „Blutgefäßkammer“ soll ein erster Schritt zur tierversuchsfreien Erforschung von Blutgefäßerkrankungen und deren Folgen sein, um Tierversuche in diesem Bereich künftig vollständig zu ersetzen.
Die synergetische wissenschaftliche und technische Unterstützung durch das entsprechende interdisziplinäre Team von Assoz.-Prof. Jens Hartmann und Univ.-Prof. Stefan Nehrer an der Universität für Weiterbildung soll zur erfolgreichen Umsetzung des geplanten Projekts beitragen.
Projektinfo:
Titel: Entwicklung eines neuen humanbasierten ex-vivo-
Blutgefäßmodells – Glykokalyx
Laufzeit: 2025-2027
Fördergeber: Technopolprogramm Niederösterreich/EFRE
(Projektnummer: WST3-F-5030664/039-2024)
Projektverantw.: Dipl.-Ing. Christoph Bauer, PhD BSc BA, Zentrum für
Regenerative Medizin der Universität für Weiterbildung Krems
Tags